
扫码添加微信,获取更多半导体相关资料
摘要
锗的溶解在过氧化氢水从3到90%H2O2和pH从1到9已经研究在温度从25~90~已经发现溶解率保持不变的溶液重量3-30%的H2O2低pH,然后减少随着H2O2增加。所提供的内容。pH4以上的反应高度依赖于pH,这种pH依赖性随H2O2浓度的变化而变化。这说明在pH值为5及以上时,低、高H2O2浓度溶液的速率控制步骤可能不同。提出了解释这种情况的反应机制。
介绍
使用过氧化氢溶液作为锗的最终清洁蚀刻是半导体行业的一个既定实践。采用稀过氧化氢水溶液作为过氧化氢水溶液。Miller用pH5的体积过氧化氢溶液测定了不同温度下锗在3.4%下的溶解速率。本研究是为了更好地了解溶解反应的机理,并确定其对过氧化氢浓度、温度和溶液pH的依赖性。研究了锗的电阻率、电阻率类型和晶体完美度对溶解速率的影响。
实验
所用样品为1x1.5x0.010in。单晶n型和p型锗的电阻率为2-6欧姆cm。1样品与~111~平面的主要表面在1度内,并用氧化铝包面制备。切片上的随机面积测量显示,表观表面积的变化小于2%。对单个样品的电阻率测量显示变化小于5%。蚀刻前,每个样品用三氯乙烯、氯仿和甲醇脱脂,干燥,用氢氟酸清洗,并用电阻率高于15兆高姆的蒸馏去离子水冲洗。干燥后,样品被称重到最接近的百分之一毫克,厚度用百分盘微米测量到最接近的十分之一毫米。样品被放置在小型钝化不锈钢丝篮中,并单独蚀刻在含有150毫升溶液的单独烧杯中,每个烧杯保持在176的温度内。没有使用搅拌蚀刻剂。反应热较低,通过烧杯迅速耗散,从而在所有情况下有效地进行反应。在每个蚀刻期结束时,锗样品为在大量的去离子水中快速去除和淬灭。冲洗和干燥后,测量样品并再次称重。样品在相同的溶液中蚀刻多次,以建立一个恒定的蚀刻速率。假设在去除工作损伤层后达到的恒定蚀刻速率接近于真实的蚀刻速率。由于每蚀刻期间厚度的减少低于刻刻在高浓度过氧化氢的灵敏度,蚀刻速率的大部分数据以每平方厘米小时毫米为单位,以便从低到高过氧化氢浓度一致。
结果
本节研究了n型和p型非简并锗以及简并n型锗的溶解速率与溶液温度的溶解速率与溶液temperature的关系。
表I给出了通过这些研究确定的不同溶液pH和重量%的H2O2水溶液中的n型锗溶解的估计活化能值。p型锗的测定值非常相似。从这些数据可以看出,在pH5及以上的活化能约为10.5千卡/摩尔,在pH4及低于该值约6.5千卡/摩尔。对于n型和p型电导率的锗以及高达10~原子/cm~的低和高杂质水平的活化能相同。溶解速率与pHoS溶液的关系在图中5.
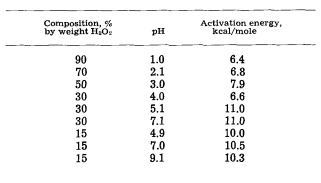
表一 使用n型锗(2-6)欧姆厘米的各种H2O2蚀刻成分的活化能
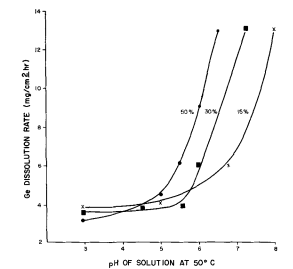
图5 三种H20=浓度下锗溶解率对溶液pH的依赖关系
讨论
从实验结果可以明显看出:(a)即使在高温下,H2O2水溶液中H2O2的溶解率为3~30%;(b)在浓度范围为30%以上H2O2时,随着~~含量的增加而线性下降;(c)在pH范围超过5时,有一定的临界pH值,该值随pH的增加而线性增加,如图所示。 2.这个临界pH随H2O2浓度而变化,如图所示。5和6;(d)在pH4的溶液中,反应的活化能约为6.5千卡/摩尔,pH5及以上的反应活化能约为10.5千卡/摩尔。由米勒给出的活化能(2)在pH5的3%H2O2的溶液中为11千卡/摩尔;(e)p型锗蚀刻速率比n型锗略快;(f)具有缺陷严重且杂质浓度高的锗的溶解率高于非简并锗,具有更好的结晶完美的基础上。根据以上实验结果,提出了锗在中溶解的两步机理。
实验中的困难限制了可以获得控制溶解的条件。例如,在高温下,在30%H2O、pH大于9的溶液或在90%H2O2浓度溶液中不能进行实验。H2O2解决方案的极端不稳定性使得它不可能保持恒定的温度和位置。然而,在25~以下的温度下进行实验是可行的,为了获得更定量的结果,需要在更低的温度下进行进一步的实验工作。
结论 略
文章全部详情,请加华林科纳V了解:壹叁叁伍捌零陆肆叁叁叁